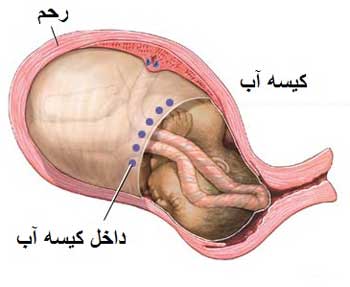
علت آمبولی مایع آمنیوتیک احتمالا ترکیبی از افزایش فشار مایع آمنیوتیک و وجود یک نقص در نزدیکی محل جفت است، که به گردش خون مادری راه دارد …
آمبولی مایع آمنیوتیک یا Amniotic fluid embolism یا AFE یکی از موقعیت های اورژانسی نادر است که در آن مایع آمنیوتیک، سلول های جنینی و یا مو وارد چرخه خون مادر می شود و می تواند مشکلات قلبی تنفسی را برای او در پی داشته باشد.
در سال ۱۹۴۱ Steiner و Luschbaugh، بعد از این که بقایای جنین را در چرخه ریوی خانمی یافتند که در طول زایمان جان خود را از دست داده بود، AFE را برای نخستین بار شناسایی کردند.
داده ها نشان می دهد این فرایند بیشتر شبیه آنافیلاکسی است تا آمبولی از این رو اصطلاح سندرم آنافیلاکتوئید بارداری (anaphylactoid syndrome of pregnancy) مناسب تر خواهد بود زیرا بافت جنینی و یا اجزای مایع آمنیوتیک عموما در فرد مبتلا به علائم AFE یافت نمی شود.
تشخیص AFE عموما زمانی انجام می شد که کالبد شکافی، سلول های سنگفرشی جنین را در چرخه ریوی مادر نشان دهد، اما سلول های سنگفرشی جنین معمولا در گردش خون بیمارانی یافت می شد که به این سندرم مبتلا نیستند. در فردی که بیمار شناخته می شود نمونه به دست آمده از پورت دیستال شریان ریوی که حاوی سلول های سنگفرشی جنین می باشد حاکی از AFE است اما تشخیص قطعی نخواهد بود. تشخیص لزوما بر پایه تظاهرات بالینی خواهد بود. سایر علل مربوط به ناپایداری همودینامیک نباید نادیده گرفته شود.
علت آمبولی مایع آمنیوتیک:
علت آمبولی مایع آمنیوتیک یا AFE به خوبی درک نشده است. بر اساس توضیحات موجود، فرض می شود که مایع آمنیوتیک و سلول های جنینی وارد چرخه خون مادر شود و احتمالا آنتی ژن های جنینی می تواند منجر به ایجاد واکنش آنافیلاکتیک شود. اما ترکیبات جنینی همیشه در گردش خون مادرانی با علائم AFE یافت نمی شود. وجود ترکیباتی با منشا جنینی اغلب در خانم هایی یافت می شود که به AFE مبتلا نیستند.
Benson و همکارانش دو فرضیه را در ارتباط با پاتوفیزیولوژی AFE تست کردند ۱) علائم بالینی ناشی از دگرانولاسیون mast cell هایی می باشد که با آزاد شدن هیستامین و تریپتاز (tryptase) همراه است و یا ۲) علائم بالینی ناشی از فعال سازی مسیر کمپلمان (complement) می باشد. ۹ مورد خانم مبتلا به AFE با ۲۲ خانم با زایمان نرمال مورد مقایسه قرار گرفتند. سرم به دست آمده از بیماران مبتلا به AFE در ۱۴ ساعت شروع علائم جمع آوری و منجمد شد. نمونه ادرار، ۱۲ تا ۲۴ ساعت بعد از شروع علائم جمع آوری شد. در افراد گروه شاهد میزان کمپلمنت به هنگام وارد شدن در بیمارستان، در طول زایمان و یک روز بعد از زایمان اندازه گیری شد.
۶ مورد از ۹ خانم مبتلا به AFE جان خود را از دست دادند و همه ۹ نفر به دلیل انعقاد درون عروقی منتشر شده یا disseminated intravascular coagulation یا DIC به انتقال خون نیاز داشتند. ۷ نفر از خانم ها شواهدی مبنی بر دگرانولاسیون نشان ندادند (هیستامین ادراری و یا تریپتاز سرمی). در مقایسه با گروه شاهد بعد از زایمان، میزان کمپلمنت در گروه مبتلا به AFE به شدت کاهش یافت. C3 در گروه AFE 44 بود در حالی که در گروه شاهد ۱۱۷٫۲ بود. C4 در گروه AFE 10.7 و در گروه شاهد ۲۹٫۴ بود. این تفاوت ها به لحاظ آماری معنی دار بود و نشان می داد که فعال سازی کمپلمان در پاتوفیزیولوژی AFE نقش مهمی ایفا می کند.
Farrar و Gherman موردی از خانم ۴۰ ساله را گزارش کردند که حین زایمان دچار اریتم حاد صورت، تشنج، هایپوکسی، ایست قلبی، DIC و نهایتا مرگ شده بود (که البته زایمان اول ایشان نبود). بعد از کالبد شکافی، سلول های سنگفرش جنینی و ترمبوز فیبرین در ریه این فرد یافت شد. دو ساعت بعد از شروع علائم خون فرد گرفته شد و میزان تریپتاز سرمی ۴٫۷ نانوگرم در میلی لیتر بود (مقدار نرمال آن کمتر از یک نانوگرم در میلی لیتر می باشد).
گزارشی از Marcus و همکارانش در دست است که نشان می دهد AFE بعد از پارگی خود به خودی غشا ایجاد شده و با استفاده از رنگ آمیزی Giemsa، اثبات شد میزان دگرانولاسیون در بافت های ریه افزایش نداشته است. مقدار سرمی تریپتاز ۱۱٫۴ نانوگرم در میلی لیتر بود (مقدار نرمال کمتر از ۱۱٫۴ نانوگرم در میلی لیتر).
رویداد آغازی به خوبی شناخته شده نیست. اما معمولا در طول زایمان مایع آمنیوتیک و بقایای جنینی و یا ترکیبی که هنوز ناشناخته است وارد گردش خون مادر می شود و واکنش آنافیلاکتیک وسیعی را ایجاد کرده، سیستم آبشاری کمپلمان را فعال می سازد و یا هر دوی این اتفاقات با هم ایجاد شود. پیشرفت این پروسه در دو مرحله اتفاق می افتد. در فاز یک، وازواسپاسم شریان ریوی همراه با هایپرتنشن ریوی و افزایش فشار بطن راست سبب بروز هایپوکسی می شود. هایپوکسی سبب آسیب مویرگی به میوکارد و آسیب مویرگی به ریه، نارسایی قلبی و سندرم دیسترس تنفسی حاد می شود. خانم هایی که این حوادث را پشت سر می گذارند وارد فاز دوم خواهند شد. در این مرحله خونریزی شدیدی اتفاق می افتد که با ضعف رحم و DIC همراه است اما اختلال انعقادی کشنده می تواند از تظاهرات بالینی اولیه باشد.
آمبولی مایع آمنیوتیک یا AFE حادثه ای غیرقابل پیش بینی و غیرقابل پیشگیری است که علت ناشناخته ای دارد. آمار ها نشان می دهد ۴۱ درصد این بیماران سابقه آلرژی داشته اند.
احتمال ابتلا به آمبولی مایع آمنیوتیک در چه کسانی بیشتر است؟
سابقه داشتن چندین زایمان، افزایش سن مادر، جنین پسر و تروما. در بررسی گذشته نگری که انجام شده است در یک دوره ۱۲ ساله ۱۸۰ مورد AFE اتفاق افتاده که ۲۴ مورد کشنده بوده، القای زایمان ریسک AFE را افزایش داده بود. در همان بررسی نشان داده شد AFE با انجام سزارین، زایمان واژینال که به طریق جراحی انجام می شود (Operative vaginal delivery )، جدا شدن (abruption)، جفت سر راهی، پارگی رحم، پارگی سرویکس و سابقه داشتن چندین زایمان ارتباط مثبتی داشته است. (Operative vaginal delivery زایمان طبیعی است که در آن جراح با استفاده از دستگاه خلا و یا انبر جراحی نوزاد را خارج می کند و ممکن است این پروسه با هل دادن مادر همراه باشد و یا نباشد).
در تحقیقی متشکل از ۱۸۲ بیمار نشان داده شد ارتباط قوی بین AFE و بیماری های کلیوی، جفت سر راهی، پلی هیدرآمینوس، اکلامپسیا و جدا شدن زودرس جفت هم چنین روش هایی مانند amnioinfusion، انجام سزارین کلاسیک و اتساع و کورتاژ وجود دارد. نشان داده شده است که ریسک AFE متناسب با سن مادر افزایش می یابد و بعد از ۳۹ سالگی احتمال بروز آن در بیشترین حالت است.
اپیدمیولوژی (آمارهای بین المللی و ایالات متحده آمریکا):
شیوع AFE یک مورد از هر ۸۰۰۰ تا ۳۰۰۰۰ بارداری تخمین زده می شود. شیوع واقعی AFE نامعلوم است زیرا تشخیص غیر دقیق و گزارش های متناقض از موارد غیرکشنده در دست است.
شیوع بین المللی AFE مشابه آمار به دست آمده در ایالات متحده در آمریکاست.
پیش آگهی:
شیوع مرگ میر در اثر AFE بالاست.
عوارض:
ادم ریوی یکی از مشکلات شایع در بازماندگان است. باید توجه زیادی به مایع ورودی و خروجی این افراد داشت.
نارسایی قلب چپ نیز ممکن است اتفاق بیفتد. برخی منابع پشتیبانی اینوتروپیک را توصیه می کنند.
درمان DIC می تواند با اجزای خونی صورت پذیرد. فاکتور فعال شده VIIa برای خونریزی شدید استفاده می شود. گزارش شده است که آمبولیزاسیون دو طرفه شریان رحمی در کنترل خون از دست رفته در دو مورد موفقیت آمیز بوده است.
سابقه:
آمبولی مایع آمنیوتیک معمولا در حین وضع حمل اتفاق می افتد اما در طول سقط، بعد از تروما در ناحیه شکم و در طول آمنیوانفوزیون (amnioinfusion) نیز اتفاق افتاده است.
یک خانم در اواخر مراحل زایمان به طور حادی دچار dyspneic (تنفس دشوار) و افت فشار می شود، او دچار تشنج و ایست قلبی شده و خونریزی شدیدی نیز به دنبال DIC اتفاق افتاده و در نهایت مرگ واقع می شود. اغلب بیماران در طول یک ساعت شروع علائم جان خود را از دست می دهند.
هیچ آزمایش تشخیصی قطعی وجود ندارد. ایالات متحده آمریکا و انگلیس چهار معیار تشخیصی را تعریف کرده اند و برای تشخیص باید همه چهار معیار وجود داشته باشد:
هایپوتنشن حاد یا ایست قلبی
هایپوکسی حاد
خونریزی شدید و یا اختلالات انعقادی در غیاب سایر توضیحات
همه این موارد در طول زایمان، سزارین، اتساع و تخلیه یا در طول ۳۰ دقیقه بعد از زایمان اتفاق بیفتد و توضیح دیگری برای آن وجود نداشته باشد.
علائم فیزیکی:
در گزارشات نشان داده شده است بیماران مبتلا به آمبولی مایع آمنیوتیک دچار تنگی نفس حاد شده برخی اوقات سرفه نیز وجود دارد و به دنبال آن هایپوتنشن نیز اتفاق می افتد.
علائم زیر می تواند احتمالی برای وجود AFE باشد:
هایپوتنشن: فشار خون ممکن است با از دست رفتن اقدامات دیاستولیک به شدت افت کند.
دشواری در تنفس و یا Dyspnea: تنگی نفس و دتاکی پنه ممکن است اتفاق افتد.
سرفه: سرفه می تواند تظاهری از تنگی نفس باشد.
سیانوز: مادامی که هیپوکسی ایجاد می شود، سیانوز محیطی و سیستمیک نیز اتفاق می افتد و تغییراتی در غشای موکوزی ظاهر می شود.
برادیکاردی جنینی: در پاسخ به هیپوکسی، ضربان قلب جنین به کمتر از ۱۱۰ ضربان در دقیقه (bpm) کاهش می یابد. اگر این کاهش به مدت بیش از ۱۰ دقیقه یا بیشتر به طول انجامد برادیکاری خواهد بود. ضربان ۶۰bpm به مدت ۳ تا ۵ دقیقه می تواند نشان دهنده برادیکاردی ترمینال باشد.
ادم ریوی: این ضایعه در رادیوگراف قفسه سینه نشان داده می شود.
ایست قلبی
ضعف رحم: ضعف رحم منجر به خونریزی شدید بعد از زایمان می شود. ناتوانی رحم با استفاده از ماساژ دودستی قابل تشخیص است (bimanual massage).
خونریزی شدید یا اختلال انعقادی در صورت وجود هیچ گونه توضیح دیگری (DIC در ۸۰ درصد بیماران اتفاق می افتد).
تغییر در وضعیت ذهنی، گیجی، تحریک
ملاحظات تشخیصی:
در مورد رادیوگراف های به دست آمده از قفسه سینه، یافته های جانبی، خلفی قدامی معمولا اختصاصی نیست اما شواهد مبنی بر ادم ریوی ممکن است قابل مشاهده باشد.
بیمار دچار AFE باید در واحد مراقبت های ویژه یا ICU بستری شوند. درمان پشتیبان عبارت است از:
استفاده از اکسیژن برای حفظ اشباع نرمال. در صورت لزوم اکسیژن رسانی می تواند به صورت Intubate انجام شود.
آغاز احیای قلبی ریوی(CPR) در صورت بروز ایست قلبی تنفسی. اگر بیمار به احیا پاسخ نداد، زایمان سزارین PMCD انجام می شود (perimortem cesarean delivery).
درمان هایپوتنشن با استفاده از کریستالوئید (crystalloid) و محصولات خونی. استفاده از pressor ها در صورت لزوم
مانیتور کردن مستمر نوزاد
در نظر داشتن کاتتریزاسیون (catheterization) شریان ریوی در بیمارانی که از نظر همودینامیک ناپایدار هستند.
درمان انعقادی با FFP در صورت طولانی شدن aPTT، cryoprecipitate در صورتی که میزان فیبرینوژن کمتر از ۱۰۰ میلی گرم در دسی لیتر باشد و تزریق پلاکت در صورتی که مقدار پلاکت کمتر از ۲۰۰۰۰ در میکرولیتر باشد.
لیم و همکارانش موردی را گزارش کردند که اختلال انعقادی با استفاده از فاکتور نوترکیب فعال شده VIIa درمان شد. در مواردی که خونریزی شدیدی اتفاق افتاده باشد دوز ۲۰ تا ۱۲۰ میکروگرم بر کیلوگرم مورد استفاده قرار می گیرد.
نشان داده شده است در بیمار مبتلا به AFE که دچار افت قلبی عروقی شده بود، همودیالیز با plasmapheresis هم چنین extracorporeal membrane oxygenation با استفاده از intra-aortic balloon counterpulsation موثر و موفقیت آمیز بوده است. (plasmapheresis روشی است که طی آن خون از بدن خارج شده و پلاسمای آن جدا می شود و باقیمانده سلول ها به جریان خون باز می گردد. این روش برای از بین بردن آنتی بادی ها در درمان شرایط خودایمنی استفاده می شود) (Extracorporeal membrane oxygenation یا ECMO نوعی بای پس قلبی- ریوی است که بدن را از بیرون پشتیبانی می کند. در این روش به واسطه ریه مصنوعی گردش خون بیمار تامین می شود).
خانم های مبتلا به AFE احتمالا به مراقبت آی سی یو نیاز خواهند داشت. نارسایی قلب چپ اتفاقی شایع است. علاوه بر این بازماندگان احتمالا دچار عوارض عصبی خواهند شد. اگر علائمی مبنی بر نقایص عصبی بروز کند مشورت با متخصص اعصاب ضروری خواهد بود.
داروها:
داروهای به کار رفته در برطرف کردن AFE به مظور تثبیت بیمار استفاده می شود. Pressor ها به منظور تثبیت فشار خون استفاده می شود، inotrpe ها انقباض را بهبود خواهد بخشید. استفاده از استروئید می تواند در فرایند ایمنی نقش داشته باشد. Uterotonic ها برای محدود کردن خونریزی بعد از زایمان استفاده می شود. (pressor با تحریک انقباض عروق خونی فشار خون را افزایش می دهد)( inotrope عاملی است که نیرو و انرژی انقباض ماهیچه های قلبی را تغییر می دهد. عواملی با اینوتروپ منفی نیروی انقباض ماهیچه ای را تضعیف می کند. عواملی با اینوتروپ مثبت قدرت انقباض ماهیچه ای را افزایش می دهد)(Uterotonic ها عواملی هستند که به منظور القای انقباض رحم به کار می روند).